BERININ-P FAKTOR IX 600 IU 1 flakon
Bölümü
Kullanılır
Kullanılır
Etkileri
Nelerdir
BERININ P 600 IU I.V. enjeksiyon/infüzyon için liyofilize toz içeren flakon Damar içine (intravenöz) uygulanır.
Etken Madde
600 IU konsantre insan koagülasyon Faktör IX içerir.
Yardımcı maddeler
Antitrombin III, heparin, aminoasetik asit, kalsiyum klorür, hidroklorik asit yada sodyum klorür, sodyum sitrat, enjeksiyonluk su (çözücü).
Bu ilacı kullanmaya başlamadan önce bu KULLANMA TALİMATINI dikkatlice okuyunuz, çünkü sizin için önemli bilgiler içermektedir.
Bu kullanma talimatını saklayınız. Daha sonra tekrar okumaya ihtiyaç duyabilirsiniz.
• Eğer ilave sorularınız olursa, lütfen doktorunuza veya eczacınıza danışınız.
• Bu ilaç kişisel olarak sizin için reçete edilmiştir, başkalarına vermeyiniz.
• Bu ilacın kullanımı sırasında, doktora veya hastaneye gittiğinizde doktorunuza bu ilacı kullandığınızı söyleyiniz.
• Bu talimatta yazılanlara aynen uyunuz. İlaç hakkında size önerilen dozun dışında yüksek veya düşük doz kullanmayınız.
Bu Kullanma Talimatında:
1. BERININ-P FAKTOR IX nedir ve ne için kullanılır?
2. BERININ-P FAKTOR IX’i kullanmadan önce dikkat edilmesi gerekenler
3. BERININ-P FAKTOR IX nasıl kullanılır?
4. Olası yan etkiler nelerdir?
5. BERININ-P FAKTOR IX’in saklanması
Başlıkları yer almaktadır.
2.BERININ-P FAKTOR IX kullanmadan önce dikkat edilmesi gerekenler
BERININ-P FAKTOR IX’i aşağıdaki durumlarda KULLANMAYINIZ
Eğer:
• BERININ P bileşimindeki her hangi bir maddeye karşı aşırı duyarlılığınız var ise bu ilacı kullanmayınız. Aşırı duyarlılığınızın olup olmadığından emin değilseniz doktorunuza danışınız. (Aşırı duyarlılık reaksiyonlarının neden olduğu yan etkiler için bakınız. bölüm 4. Bağışıklık sistemi hastalıkları)
• BERİNİN P yardımcı madde olarak heparin içermektedir. Heparin alerjik reaksiyonlara ve kan pıhtılaşmasından sorumlu olan kan hücrelerinin (trombosit) sayısında azalmaya neden olabilir. Heparin ile ilişkili daha önceden bilinen bir alerji öyküsüne sahipseniz heparin içeren ilaçları kullanmayınız. (Heparin’in neden olduğu kan hücrelerinin (trombosit) sayısındaki azalmanın sonucunda görülebilecek yan etkiler için bakınız Bölüm 4. Kan ve lenf sistemi hastalıkları)
Heparin alerjisine karşı, BERİNİN P ile tedaviye başlamadan önce ve tedaviye başladıktan sonraki ilk günde ve ilk üç hafta boyunca düzenli olarak her üç ila dört günde bir kan hücrelerinizin sayısının (trombosit) kontrol edilmesi gerekmektedir. Hatta BERİNİN P ile tedavinin bitiminde de kan hücre sayınızı kontrol ettirmelisiniz.
BERININ-P FAKTOR IX’i aşağıdaki durumlarda DİKKATLİ KULLANINIZ
Eğer:
• Faktör IX’ un tedavi edici etkisini önleyen maddeleri (antikorları) geliştirme riskine sahipseniz, BERİNİN P’ i kullandığınızda kanamanız kontrol edilemiyorsa faktör IX’ un kanamayı durdurucu etkisini önleyen antikorlar (inhibitör) geliştirmiş olabilirsiniz. Bu durumda mutlaka doktorunuza başvurmalısınız. Doktorunuz bunu doğrulamak için sizi birtakım testlere tabi tutacaktır.
Ayrıca antikor oluşumu ile alerjik reaksiyon oluşumu arasında ilişki olabileceğinden sizde herhangi bir alerjik reaksiyon oluşumunda doktorunuz tarafından antikorların varlığı açısından değerlendirileceksinizdir. (Alerjik reaksiyon belirtileri için bakınız Bölüm 4 . Bağışıklık sistemi hastalıkları)
• BERININ P’ i kullandığınızda çok seyrek olarak vücuttaki herhangi bir damardan kopan pıhtı parçasının başka bir damarınızı tıkaması (tromboembolik) riski oluşabilir. Bu riskin oluşturacağı yan etkilerin görülmesi halinde doktorunuza başvurmalısınız. (Yan etkiler için bakınız. bölüm 4. Damar hastalıkları.)
Bu riski arttıran faktörler;
– Daha önce koroner kalp hastalığı ya da kalp infarktüsü geçirdiyseniz,
– Karaciğer hastalığınız var ise,
– Ameliyat sonrasında BERİNİN P kullanmanız gerekiyorsa,
– Yeni doğan çocuklarda BERİNİN P kullanımında,
– Yaygın damar içi pıhtılaşma riskinde (DIC)
Yukarıda bahsedilen durumlardan herhangi birinin sizde mevcut olması halinde doktorunuzla bu konuyu tartışmalısınız.
• BERININ P’ nin damarınızın içine verilmesi sırasında bir reaksiyon oluştuğunu hissederseniz (örneğin; ilacın verildiği yerde kızarıklık, şişme, kaşıntı vs…) derhal doktorunuza bildiriniz. Doktorunuzun kararına göre ilacın damarınızın içine verilme hızı yavaşlatılabilir ya da tamamen durdurulabilir.
Bu uyarılar, geçmişteki herhangi bir dönemde dahi olsa sizin için geçerliyse lütfen doktorunuza danışınız.
BERININ-P FAKTOR IX’in yiyecek ve içecek ile kullanılması
BERININ-P FAKTOR IX’in yiyecek ve içecek ile kullanılması
Hamilelik
İlacı kullanmadan önce doktorunuza veya eczacınıza danışınız.
BERININ P’ nin gebelik döneminde kullanılmasının güvenli olup olmadığı henüz tam olarak bilinmemektedir. Doktorunuz, bu ilacı kullanmanızın kesinlikle gerekli olduğuna karar vermiş ve bunu size bildirmiş ise, hamile iken bu ilacı kullanmanız önerilebilir. Ancak buradaki tüm sorumluluk size ve doktorunuza aittir.
Tedaviniz .sırasında hamile olduğunuzu fark edersiniz hemen doktorunuza veya eczacınıza danışın.
Emzirme
İlacı kullanmadan önce doktorunuza veya eczacınıza danışınız.
BERININ P’ nin emzirme döneminde kullanılmasının güvenli olup olmadığı henüz tam olarak bilinmemektedir. Doktorunuz, bu ilacı kullanmanızın kesinlikle gerekli olduğuna karar vermiş ve bunu size bildirmiş ise, emzirme döneminde bu ilacı kullanmanız önerilebilir.
Araç ve makina kullanımı
Araç ve makina kullanımı
BERININ-P FAKTOR IX’in içeriğinde bulunan bazı yardımcı maddeler hakkında önemli bilgiler
Bu tıbbi ürün her dozunda 24 mg (1,043 mmol) sodyum içermektedir. Kontrollü sodyum diyeti alan kişilerde bu durum göz önünde bulundurulmalıdır.
Bu tıbbi ürün her dozunda 5-25 IU heparin içermektedir. Heparin alerjik reaksiyonlara ve kan pıhtılaşma sistemini etkileyen kan hücrelerinin sayısının azalmasına neden olabilir. Heparin ile ilişkili alerji öyküsü olan hastalarda heparin içeren ilaçlar kullanılmamalıdır.
Diğer ilaçlar ile birlikte kullanımı
BERİNİN P diğer tıbbi ürünlerle karıştırılmamalıdır ve ilacın infüzyonu ayrı bir damardan yapılmalıdır.
Eğer reçeteli yada reçetesiz herhangi bir ilacı şu anda kullanıyorsanız veya son zamanlarda kullandınız ise lütfen doktorunuza veya eczacınıza bunlar hakkında bilgi veriniz.
5.BERININ-P FAKTOR IX’in saklanması
BERININ P’ i çocukların göremeyeceği, erişemeyeceği yerlerde ve ambalajında saklayınız.
BERİNİN P, 25 °C’ nin altındaki oda sıcaklığında saklayınız. Dondurmayınız! Donmuş ürünü çözüp kullanmayınız.
BERİNİN P kapalı karton kutusu içinde muhafaza edilmelidir. Isı ve ışıktan korunmalıdır. Sulandırıldıktan sonra derhal kullanılmalıdır. Eğer hemen uygulanmayacaksa, sulandırılan
solüsyon, sterilitesi sağlandığı takdirde, 25 °C’de oda sıcaklığında 8 saat bekletilebilir. Kullanılmayan çözeltiler uygun bir biçimde atılmalıdır.
Son kullanma tarihiyle uyumlu olarak kullanınız
Ambalajdaki son kullanma tarihinden sonra BERININ-P FAKTOR IX’i kullanmayınız.
Eğer üründe ve/veya ambalajında bozukluklar fark ederseniz BERININ-P FAKTOR IX’i kullanmayınız.
Çevreyi korumak amacıyla kullanmadığınız BERINİN P’ i şehir suyuna veya çöpe atmayınız. Bu konuda eczacınıza danışınız.
Ruhsat Sahibi:
Farma-Tek İlaç San. ve Tic. Ltd. Şti. Şerifali Mah.Bayraktar Bulvarı.Beyan Sok. No:12 Ümraniye/İstanbul
Üretim yeri: CSL Behring GmbH
AŞAĞIDAKİ BİLGİLER BU İLACI UYGULAYACAK SAĞLIK PERSONELİ İÇİNDİR. Pozoloji:
Uygulama süresi ve dozu hastanın Faktör IX eksikliğine, kanamanın yerine, miktarına ve hastanın klinik durumuna bağlıdır.
Uygulama miktarı ve uygulama sıklığı her bir bireyin klinik etkinlik düzeyine göre belirlenir.Faktör IX ilaçları nadir olarak günde birden fazla kullanımı gerektirir.
Aşağıdaki hemorajik olgularda faktör IX düzeyi o döneme ait plazma aktivitesi düzeyinin (normalin %’ si ya da IU/dL olarak) altına düşmemelidir.
Aşağıdaki tablo ameliyatlardaki ve kanamalı olgularda kullanılacak dozun miktarını belirleyebilmek için kullanılabilir:
|
Hemoraji derecesi/ Cerrahi müdahalenin tipi |
Gerekli Faktör IX seviyesi (% ya da IU/dL) |
Doz sıklığı (saat) /Tedavinin süresi (gün) |
|
Hemoraji |
||
|
Erken hemartroz Kas içi kanama, Ağız boşluğunda kanama |
20 – 40 |
Her 24 saat de bir kanama duruncaya veya iyileşme sağlanıncaya kadar infüzyon tekrarlanır. |
|
Daha yoğun hemartroz, Kas içi kanama, hematom |
30 – 60 |
Acısı ve kanamanın şiddeti azalıncaya kadar 3 -4 gün boyunca infüzyon her 24 saat de bir tekrar edilir. |
|
Hayatı tehdit eden hemoraji |
60 – 100 |
iyileşme gerçekleşinceye kadar 8 ila 24 saatte de bir infüzyon tekrar edilir. |
|
Cerrahi müdahale |
||
|
Diş çekilmesi gibi küçük müdahaleler. |
30 – 60 |
Her 24 saat de bir en az 1 gün boyunca iyileşme gerçekleşinceye kadar infüzyon tekrar edilir. |
|
Büyük cerrahi müdahalelerde |
80 – 100 (preoperatif ve postoperatif) |
Yara kafi derecede iyileşene dek infüzyon 8 ila 24 saat de, tedavinin devam ettiği 7 gün boyunca Faktör IX aktivitesi % 30 – 60 (IU/dL) olacak şekilde ayarlanır. |
Tedavinin devam ettiği sırada tekrarlanan infüzyon periyodu ve uygun görülen faktör IX seviyesi belirtilmelidir. Özellikle majör cerrahi girişim olgularında, yerine koyma tedavisinin koagülasyon analiziyle (plazma faktörü IX aktivitesi) titiz olarak izlenmesi zorunludur. Faktör IX’ a cevap verme durumu bireylerde farklılık gösterebilir.
Ciddi hemofili B hastalığı olanlarda kanamaya karşı uzun süreli profilaksi için 3 ila 4 günlük aralıklarla, vücut ağırlığının her kg. için 20 ila 40 IU faktör IX verilmelidir. Eğer gerekiyorsa başka tedavi önlemleri de alınmalıdır.
Bazı durumlarda özellikle genç hastalarda dozaj aralıklarını kısaltmak yada yüksek doz uygulamak gerekebilir.
Hastalar, faktör IX inhibitörlerinin gelişimi açısından izlenmelidir. Eğer beklenen faktör IX aktivite plazma seviyesi elde edilemezse ya da uygun doz ile kanama kontrol altına alınmazsa faktör IX inhibitörlerinin varlığına karar vermek için analiz yürütülmelidir. Hastada yüksek seviyede inhibitör varlığında, faktör IX tedavisi etkisiz olabilir ve diğer tedavi yöntemleri göz önünde bulundurulmalıdır. Bazı hastaların tedavisi hemofili ile ilgili deneyimleri çok olan doktorlar tarafından yürütülmelidir.
Uygulama şekli:
Genel talimatlar:
Çözelti berrak veya hafif opak olmalıdır. Uygulama öncesi filtre edildikten/çekildikten sonra (aşağıya bakınız) hazırlanmış ürün çökelti maddesi veya renk bozulmasına karşı incelenmelidir. Kalıntı/parçacık içeren veya berrak olmayan çözeltileri kullanmayınız. Mix2Vial setini içeren filtreler artık içeren kalıntı ya da parçacıkları tamamiyle söker. Filtrasyon dozaj hesaplarım etkilemez. Çözeltiyi filtrasyondan sonra da toz parçacıkları yada partiküller içeriyorsa kullanmayınız.
Hazırlanma ve enjektöre çekilme aseptik şartlarda gerçekleştirilmelidir.
Uygulama sonrası kullanılmayan ürün veya atık madde, yerel gerekliliklere uygun şekilde bertaraf edilmelidir.
Hazırlanması:
Çözücüyü oda sıcaklığına getiriniz. Toz ve çözücü flakonlannın kapaklarının çıkarıldığından ve stoperlerin aseptik bir solüsyonla silinerek Mix2Vial paketinin açılmasından önce kendiliğinden kuruduğundan emin olunuz.
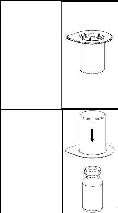
1
2
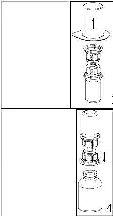
1.Kapağı soyarak Mix2Vial paketini açınız. Mix2Vial’ i blister paketinden çıkarmayınız.
2.Seti paketten çıkarınız, her iki uçtaki çentiklere dokunmamaya özen gösteriniz. Çözücü flakonu düz ve temiz bir yüzeye yerleştiriniz ve flakonu sıkıca tutunuz. Blister paketi ile birlikte aldığınız Mix2Vial setinin mavi ucunu çözücü flakonun stoperinin üzerine yerleştiriniz.
3.Mix2Vial setinden blister paketi kenarından tutarak dikkatlice sökünüz. Mix2Vial setini değilde sadece blister paketi çıkardığınızdan emin olunuz.
4.Toz flakonunu bir yüzeyde sıkıca tutarak, setin iliştirildiği çözücü flakonunu ters çevirin ve transparan adaptörü toz flakonunun stoperinin üzerine yerleştirin. Çözücü otomatik olarak toz flakonunun içine geçecektir.
5.Bir elle Mix2Vial setinin kenarından diğer ellede seyrelticinin kenarından ürünü kavrayarak iki parça içerisindeki seti vidalarından cevirerek açınız ve ürün çözülürken aşırı köpük oluşumundan kaçınınız. Mavi Mix2Vial adaptörüne bağlanmış olan seyreltici flakonu çıkarınız.
|
Ç |
W |
6.Tozun tam olarak çözündüğünden emin olmak için transparan adaptörlü ürün flakonunu nazikçe döndürerek çalkalayınız. Flakonu sallamayınız. Boş ve steril bir şırıngaya hava çekiniz. Toz flakonu yukarıya doğru dururken şırıngayı Mix2Vial setine bağlayınız. Havayı toz flakonunun içine enjekte ediniz. |
|
|
İP7 |
7.Şırınganın pistonunu basılı tutarak sistemi baş aşağı çeviriniz ve konsantreyi, pistonu yavaşça geriye çekerek şırıngaya alınız. |
||
|
oo |
8.Konsantre, şırınganın içerisine dolduktan sonra, şırıngayı sıkıca tutarak (şırınganın pistonu halen aşağı bakacak şekilde) Mix2Vial setini şırıngadan ayırınız. |
Ürün dolu şırangaya kanın girmediğinden emin olunuz.
Hazırlanan çözelti hastaya rahat edebileceği bir yerde yavaş intravenöz oranda infüzyon ya da damar içerisine enjeksiyon şeklinde uygulayınız. Enjeksiyon yada infüzyon oranının dakikada 2 mL’ i geçmemesine dikkat edilmelidir.
Vücut ağırlığının kg’ ı başına 100 IU’ den daha fazla uygulanmaması önerilmektedir. Ürünle dolu olan flakon ve kaplara hiç kan girmemesine dikkat edilmelidir.
Hasta oluşabilecek herhangi bir reaksiyona karşı izlenmelidir. BERİNİN P ile ilgili bir reaksiyon oluşması halinde infüzyon oranı hastanın klinik durumuna göre azaltılmalı yada durdurulmalıdır (bkz. Bölüm 4.4).
2.BERININ-P FAKTOR IX nedir ve ne için kullanılır?
• BERİNİN P 5 mL çözelti hazırlamak için liyofilize toz içeren flakon ve enjeksiyonluk su içeren çözücü flakon ile 1 filtre transfer aracı (Mix2Vial) içeren ambalajlarda kullanıma sunulmuştur.
• BERININ P Hemofili B hastalığının tedavisinde kullanılmaktadır. Hemofili B, kanın pıhtılaşması için gerekli pıhtılaşma faktörlerinden faktör IX seviyesinin düşmesiyle gelişen, yaşa bağlı olan, kalıtsal bir hastalıktır. Bu durum eklem yerlerinde, kaslarda yada iç organlarda kendiliğinden yada bir kaza veya cerrahi bir müdahale sonucunda durdurulamayan aşırı kanamaya neden olur. BERININ P kanın pıhtılaşması için gerekli olan faktör IX' u dolaşımda yerine koyarak kanamayı durdurur.
BERININ P aşağıda belirtilen durumların tedavisinde kullanılır:
Doğuştan faktör IX eksikliği (Hemofili B) olan hastalarda kanamaların önlenmesinde ve tedavisinde kullanılır.
3.BERININ-P FAKTOR IX nasıl kullanılır ?
Uygun kullanım ve doz/uygulama sıklığı için talimatlar
Doktorunuz hastalığınıza bağlı olarak ilacınızın dozunu belirleyecek ve size uygulayacaktır.
Uygulama yolu ve metodu
• BERİNİN P kullanıma hazır hale getirildikten sonra size, deneyimli sağlık personeli tarafından rahat edebileceğiniz bir yerde toplardamarınızdan birine yavaş enjeksiyon yoluyla verilecektir.
• Ürün hazırlandığında uygulamadan önceki sıcaklığı oda ya da vücut sıcaklığında olmalıdır.
Çocuklarda kullanımı
BERİNİN Pv nin çocuklarda doz ayarlaması ile ilgili yeterli deneyimler bulunmamaktadır. Ancak çocuklarda dozun ve infüzyon hızının dikkatli bir şekilde ayarlanması ile kullanılabilir.
Yaşlılarda kullanımı
Yaşlılarda kullanımı
Özel kullanım durumları
Böbrek ve karaciğer fonksiyon bozukluğunuz bulunuyorsa, bu ilacı kullanmadan önce doktorunuza söyleyiniz ve doktorunuzun talimatlarına uyunuz. Böbrek ve /veya karaciğer yetmezliği olan hastalarda BERİNİN P doktorun belirleyeceği çok düşük konsantrasyonlarda ve pratik olarak mümkün olabilecek en yavaş infüzyon hızında verilir. Böbrek fonksiyon testleri de düzenli olarak yapılmalıdır.
Eğer BERİNİN P' nin etkisinin çok güçlü veya zayıf olduğuna dair bir izleniminiz var ise doktorunuz veya eczacınız ile konuşunuz.
Kullanmanız gerekenden daha fazla BERININ-P FAKTOR IX kullanırsanız
Yaşlılarda kullanımı
BERİNİN P' den kullanmanız gerekenden fazlasını kullanmışsanız bir doktor veya eczacı ile konuşunuz.
BERININ-P FAKTOR IX'i kullanmayı unuttuysanız
Unutulan dozları dengelemek için çift doz almayınız.
BERİNİN P deneyimli sağlık personeli tarafından uygulanacağından, böyle bir durumun oluşmaması için gereken önlemler alınacaktır.
BERININ-P FAKTOR IX ile tedavi sonlandırıldığında oluşabilecek etkiler
BERİNİN P ile tedavinin sonlandırılmasına bağlı bir yan etki beklenmemektedir.
4.Olası yan etkiler nelerdir ?
Tüm ilaçlar gibi BERININ-P FAKTOR IX’in içeriğinde bulunan maddelere duyarlı olan kişilerde yan etkiler olabilir.
Yan etkiler aşağıdaki kategorilerde gösterildiği şekilde sıralanmıştır. Çok yaygın :10 hastanın en az 1 inde görülebilir.
Yaygın : 10 hastanın birinden az, fakat 100 hastanın birinden fazla görülebilir.
Yaygın olmayan :100 hastanın birinden az, fakat 1000 hastanın birinden fazla görülebilir. Seyrek : 1.000 hastanın birinden az görülebilir.
Çok seyrek :10.000 hastanın birinden az görülebilir.
Kan ve lenf sistemi hastalıkları
Çok seyrek:
• Bacaklarda varisler, şişme, deri değişiklikleri
• BERİNİN P' nin uygulandığı enjeksiyon bölgesinde deri dokularının yıkılması (kütanöz nekroz)
• Cilt içinde oluşan kanama (purpura, peteşi)
• Koyu renkli katranımsı feçes (melena) oluşumu
Bağışıklık sistemi hastalıkları
Çok seyrek:
• Vücutta yaygın sıcaklık artışı
• Deride yanma hissi, kızarıklık, kaşıntı, yaygın döküntü
• Dilde, dudakta, gırtlak bölgesinde şişlik (ödem) ve buna bağlı soluk alıp vermede güçlük
• Vücutta yaygın ödem ve morarma
• Göğüste sıkışma hissi
• Hırıltılı soluma
• Titreme
• Baygınlık hali, baş dönmesi ve koma hali varsa (anafilaktik şok). ( Ayrıca bakınız bölüm 2. BERİNİN P' i aşağıdaki durumlarda kullanmayınız).
Sinir sistemi hastalıkları
Çok seyrek:
• Baş ağrısı
• Uyuşukluk
• Huzursuzluk
• Sersemlik ve yorgunluk
Kardiyak hastalıkları
Çok seyrek:
• Kalp atımının hızlanması (taşikardi)
• Düşük tansiyon (hipotansiyon)
Damar hastalıkları
Çok seyrek:
• Bacaklarda ağrı ve şişme, yürüyememe
• Göğüste ani keskin acı hissi
• Aniden nefes almada zorluk
• Soğuk soğuk terleme
• Nefes darlığı
• Çok hızlı soluk alıp verme
• Korku hali
• Öksürük
Solunum, göğüs bozuklukları ve mediastinal hastalıkları
Çok seyrek:
• Soluk alıp vermede güçlük veya sıkıntı
• Hırıltılı soluma
Böbrek ve idrar hastalıkları
Çok seyrek:
• Göz çevrenizde, ellerinizde yada ayaklarınızda şişme (nefrotik sendrom)
Gastrointestinal hastalıkları
Çok seyrek:
• Mide bulantısı
• Kusma
Deri ve deri altı doku hastalıkları
Çok seyrek:
• Ürtiker
• Kaşıntı
• Serinlik
Kas-iskelet bozukluklar, bağ doku ve kemik hastalıkları
Çok seyrek
• Vücutta karıncalanma
Genel bozukluklar ve uygulama bölgesine ilişkin hastalıkları
Çok seyrek
• Geçici deri reaksiyonları
• Uygulama yerinde şişme, sertlik, ağrı
• Ateş
Yan etkilerin raporlanması
Kullanma Talimatında yer alan veya almayan herhangi bir yan etki meydana gelmesi durumunda hekiminiz, eczacınız veya hemşireniz ile konuşunuz. Ayrıca karşılaştığınız yan etkileri www.titck.gov.tr sitesinde yer alan “İlaç Yan Etki Bildirimi“ ikonuna tıklayarak ya da 0 800 314 00 08 numaralı yan etki bildirim hattını arayarak Türkiye Farmakovijilans Merkezi (TÜFAM)‘ne bildiriniz. Meydana gelen yan etkileri bildirerek kullanmakta olduğunuz ilacın güvenliliği hakkında daha fazla bilgi edilnilmesine katkı sağlamış olacaksınız.
